24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us
医疗器械是一个加速增长的市场,越来越多的企业以或研发,或生产,或经营的方式,参与着器械产业。特别近几年,原来专注于药品的企业也涉足甚至转型到医疗器械行业中来。
医疗器械的开发,包括医疗器械的自主研发,引进,迭代。基本上开发过程的投入是巨大的。为了保障开发的项目在研发设计,审评注册、市场运营、销售盈利的过程中顺利,研发人员应具备以下四大意识或能力,才能极大限度保障项目成功。
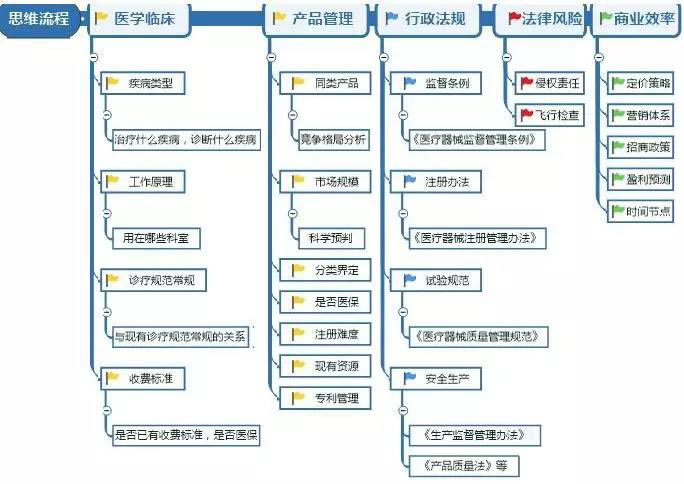
包括:第一,临床与产品意识。指具有医学临床专业素养,具备客观认识或准确调研医疗器械对临床的价值的能力,按产品管理流程推演判断。第二,行政法规意识,既对当前的行政法规规章,要熟知,对刚发布的法规,规章要掌握,对法规的趋势要了解。第三,法律风险意识。既对医疗器械在研发注册中,生产中,临床应用中,针对于这个医疗器械的法律风险要深刻掌握。第四,商业效率意识,要客观研判投资与回报周期,不盲目乐观或悲观。

第一,医学与产品意识。
预防保健,临床医疗,护理康复等医疗过程是专业性强,生命攸关的事。一个医疗器械的研发或引进,要客观看待其对患者的价值,对医务人员的价值。产品的功能是什么,相似产品有哪些,分类界定归属,注册策略,企业现有资源。这一系列重要节点的判断要依据医学科学,依据专科临床实践,依据中国国情。

第二,行政法规意识。
行政法规有《医疗器械监督管理条例》,还有专项的法规,比如要保证医疗器械的安全性和有效性,我们有《>医疗器械注册管理办法》,《医疗器械临床试验质量管理规范》;保证医疗器械生产质量,我们有《安全生产法》,《产品质量法》,还有医疗器械检验的国家标准等。行政类法规,是在产品研发的过程中,检验和审评一款医疗器械能否准许出现在中国的依据,所以熟知法规,提前研判某类产品在行政法规中,是否会遇到问题,及需要付出的代价。

第三,法律风险意识。
主要体现在产品在临床应用当中,是否存在临床试验未发现的问题,如否,会面临召回和赔偿,这种例子并不鲜见。临床试验的严格与否会直接影响着此类事件的发生概率。这个层面的法律是《侵权责任法》,如果因为产品设计问题导致医疗损害,那企业会面临非常严重的后果。所以及时研判后期的各种可能和概率,并提前在产品研发设计中就要严格规避医疗损害的风险。产品上市后,对医疗损害风险进行监督、跟踪与管理的需常态化进行。

第四,商业效率意识。
集中体现在市场测算,定价技巧和盈利预测。所有企业在项目路演的时候,PPT里都评估的非常乐观,近两年比较有名的是“中国精神病人有一亿”,“不孕不育有两亿”等,市场规模的估测都显得过于乐观,这来源于投融资方面的需要。
实际考虑要客观甚至要略保守的估计市场规模,这样筛选出来的项目,可能符合预期甚至超过预期。还有严格的时间节点意识,如果一个项目时间节点不能保证,市场上的实时变量比如竞品,技术更新等都会增加不确定性,按时交付是一种难得的能力,说到底就是踏准节奏。

总结,面对一个医疗器械项目的开发,具备临床认知和医疗产品流程管理能力;具备行政法规的了解和判断趋势的能力;具备规避医疗损害和产品质量风险的能力;具备迅速可靠的商业策划力和执行力,是为医患,为医疗机构,为社会,也为自己创造价值的全面保证。
站点声明:
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
北京飞速度医疗科技有限公司专注于医疗器械、诊断试剂产品政策与法规规事务服务,提供产品注册申报代理、临床合同(CRO)研究、产品研发、GMP质量辅导等方面的技术外包服务。
上一篇:【临床试验基础知识】破盲
下一篇:医疗器械注册退审怎么办?