24小时服务热线:19103801095
NEWS CENTER
Recommend case
contact us

上海第二类医疗器械注册(首次注册)常见发补问题包括综述资料常见发补问题、非临床资料常见发补问题、临床资料常见发补问题(含同品种临床评价)、产品说明书和标签样稿常见发补问题四个部分,具体见正文。
查看详情
《医疗器械注册质量管理体系核查指南》是现行适用的注册质量体系核查规范文件,其中对医疗器械注册自检检测事项进行了规定,一起来按具体内容。
查看详情
对于第一类医疗器械产品备案来说,产品技术要求编制可能是最具挑战性事项之一,产品技术要去包括产品的组成结构、性能指标和检验方法三个部分,本文为大家说说检验方法需要包括哪些内容。
查看详情
脊柱后路内固定系统注册产品是临床常见的植入类医疗器械,通常由纯钛及钛合金材料、聚醚醚酮、钴铬钼合金、不锈钢等材料制成。本文为大家介绍脊柱后路内固定系统产品技术要求及主要性能指标,供医疗器械注册人参考。
查看详情
适用于颈椎、胸腰椎节段(明确具体节段范围)的椎间融合术的椎间融合器临床预期用途较为统一,颈椎、胸腰椎产品可作为同一医疗器械注册单元,椎间融合器在我国属于第三类医疗器械注册产品,分类编码为13-03-04。本文为大家介绍椎间融合器注册办理流程和要求。
查看详情
对于第一类体外诊断试剂备案时,体外诊断试剂产品说明书中需要明确产品的储存条件和有效期,那法规对于产品说明书中【储存条件及有效期】有何要求呢?一起看正文。
查看详情
对于第一类医疗器械备案,产品技术要求和说明书是最必备技术资料,如何撰写产品技术要求是重中之重,本文为大家说说产品技术要求中的检验方法需要包括哪些内容。
查看详情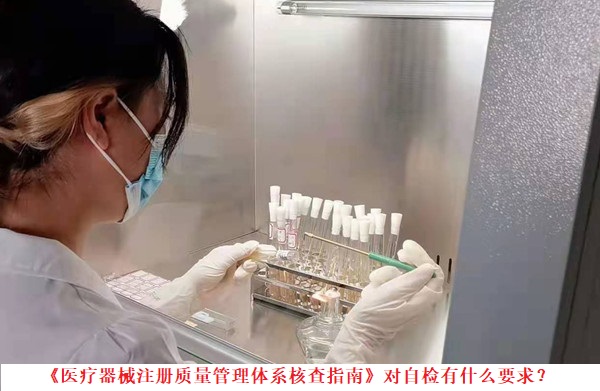
《医疗器械注册质量管理体系核查指南》是医疗器械注册质量管理体系核查的依据,亦是体系是否能够通过的判定标准之一。对于医疗器械注册人来说,了解《医疗器械注册质量管理体系核查指南》内容和要求是必要事项。本文为大家介绍指南对自检的要求。
查看详情